Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) cho biết họ đã cấp phép sử dụng khẩn cấp thuốc điều trị COVID-19 của Pfizer, Reuter đưa tin. Thuốc chỉ định cho bệnh nhân COVID-19 có nguy cơ cao tiến triển thành bệnh nặng từ 12 tuổi trở lên.
Đây là phương pháp điều trị COVID-19 bằng đường uống đầu tiên có thể được thực hiện tại nhà, giúp cung cấp một công cụ tiềm năng trong cuộc chiến chống lại biến chủng Omicron.
FDA cho biết thuốc chỉ được bán theo đơn và phải được sử dụng càng sớm càng tốt, trong vòng 5 ngày kể từ khi bắt đầu có triệu chứng.
“Việc phê duyệt Paxlovid là một cột mốc quan trọng, đánh dấu một bước nữa trong việc biến COVID-19 trở thành căn bệnh dễ kiểm soát hơn”, Amesh Adalja, một học giả cấp cao tại Viện An ninh Y tế Johns Hopkins, cho biết.
“Tuy nhiên, có hai vấn đề chính vẫn còn tồn tại: Thuốc sẽ khan hiếm trong những tuần tới và việc sử dụng tối ưu nó đòi hỏi chẩn đoán nhanh chóng”, Adalja nói thêm.
|
|
|
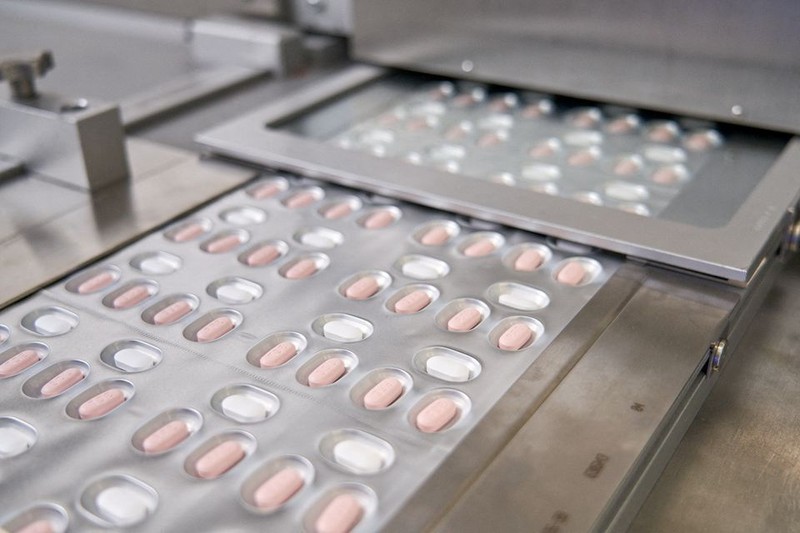
Mỹ phê duyệt thuốc viên điều trị COVID-19 của Pfizer. Ảnh: Reuters.
|
Trước đó, theo dữ liệu từ thử nghiệm lâm sàng của Pfizer, liệu pháp kháng virus đường uống Paxlovid có hiệu quả gần 90% trong việc ngăn ngừa nhập viện và tử vong ở bệnh nhân có nguy cơ cao. Dữ liệu phòng thí nghiệm gần đây cũng cho thấy thuốc vẫn giữ được hiệu quả chống lại biến chủng Omicron.
Pfizer cho biết họ có 180.000 liệu trình điều trị sẵn sàng xuất xưởng trong năm nay. Chính phủ Mỹ đã đặt hàng Paxlovid với số lượng đủ để cung cấp cho 10 triệu người, vớị giá là 530 USD một liệu trình.
Pfizer dự kiến nâng mức sản xuất năm 2022 từ 80 triệu lên 120 triệu liệu trình điều trị và cho biết họ đã sẵn sàng giao hàng tại Mỹ.
Liệu trình điều trị gồm thuốc Paxlovid và một viên ritonavir (thuốc kháng HIV) liều thấp. Ritonavir sẽ giúp thuốc Paxlovid tồn tại trong cơ thể với thời gian dài hơn.
Quyết định của FDA về việc cấp phép khẩn cấp thuốc điều trị được đưa ra trong bối cảnh Mỹ đang tăng cường biện pháp chống lại sự gia tăng các ca mắc COVID-19 do biến chủng Omicron gây ra.
Theo Minh An/Zing